|
|
 |
|
 |
|
 |
|
 |
|
 |
|
 |
|
 |
|
 |
|
 |
|
 |
|
 |
|
 |
|
 |
|
 |
|
새로운 연구에서는 종양을 죽이는 약물을 환자에게 보다 효율적으로 배포하기 위해 나노봇을 사용하는 방법을 탐구합니다. 결과는 앞으로의 치료에 큰 영향을 미칠 수 있습니다.
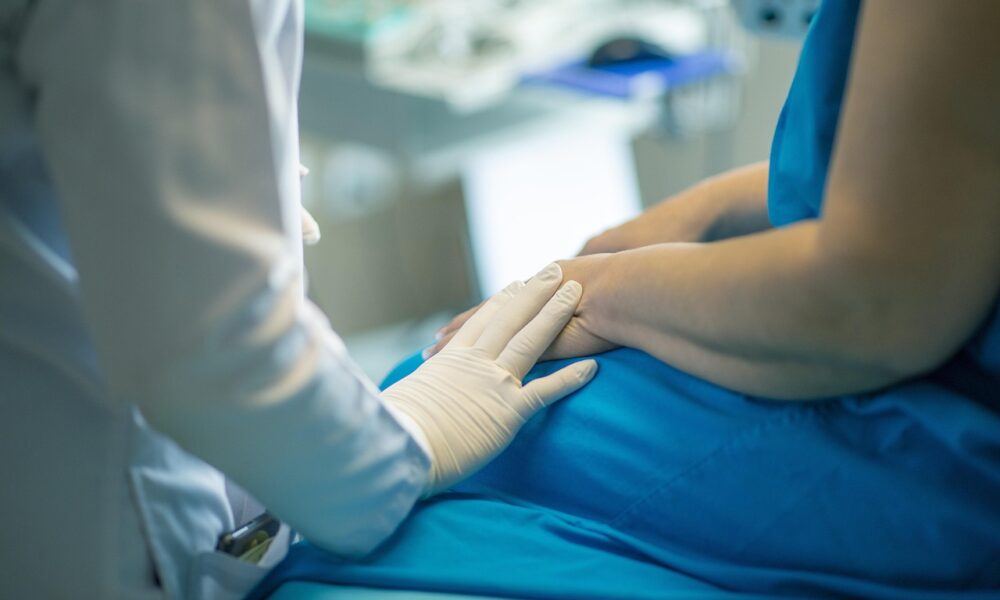
A new study explores the use of nanobots to distribute tumor-killing medications more efficiently to patients. The researchers employed tiny self-propelled machines that could penetrate deeper into bladder cancer tumors when compared to current methods. The results could have a resounding effect on treatment moving forward. Here's everything you need to know.
새로운 연구에서는 종양을 죽이는 약물을 환자에게 보다 효율적으로 배포하기 위해 나노봇을 사용하는 방법을 탐구합니다. 연구자들은 현재의 방법과 비교할 때 방광암 종양에 더 깊이 침투할 수 있는 작은 자체 추진 기계를 사용했습니다. 결과는 향후 치료에 큰 영향을 미칠 수 있습니다. 여기에 당신이 알아야 할 모든 것이 있습니다.
Bladder Cancer
방광암
Bladder cancer is one of the leading causes of death around the world. A recent study by the American Cancer Society projected around 82K people will be diagnosed with bladder cancer in 2023 alone. Of those diagnosed, around 16.5K will not survive the ordeal. As such, it's easy to see why there's considerable effort put towards helping to reduce the number of people who will be affected by bladder cancer in the coming years.
방광암은 전 세계적으로 사망의 주요 원인 중 하나입니다. 미국 암학회(American Cancer Society)의 최근 연구에 따르면 2023년에만 약 82,000명이 방광암 진단을 받을 것으로 예상됩니다. 진단을 받은 사람들 중 약 16.5K명이 시련에서 살아남지 못할 것입니다. 따라서 향후 방광암에 걸릴 사람의 수를 줄이는 데 도움이 되는 상당한 노력이 기울이는 이유를 쉽게 알 수 있습니다.
The main causes of bladder cancer are smoking, workplace exposure to carcinogens, dietary factors, genes, diesel exhaust exposure, and radiotherapy. Notably, around 75% of confirmed bladder cancer tumors are non-muscle-invasive, meaning the cancer is located only on the inner layer of cells.
방광암의 주요 원인으로는 흡연, 직장 내 발암물질 노출, 식이 요인, 유전자, 디젤 배기가스 노출, 방사선 치료 등이 있습니다. 특히 확인된 방광암 종양의 약 75%는 비근육 침윤성 종양으로, 이는 암이 세포의 내부 층에만 위치한다는 것을 의미합니다.
Current Treatment
현재 치료
The current methods of treating bladder cancer are effective and not dangerous. However, they leave lots of room for improvement. The most common procedure involves administering drugs directly to the bladder. The problem with treating bladders versus other organs is that it's designed to flush out toxins with urine constantly.
방광암을 치료하는 현재 방법은 효과적이며 위험하지 않습니다. 그러나 개선의 여지가 많이 남아 있습니다. 가장 일반적인 절차는 약물을 방광에 직접 투여하는 것입니다. 다른 기관에 비해 방광을 치료할 때의 문제점은 방광이 지속적으로 소변으로 독소를 배출하도록 설계되었다는 것입니다.
This urine, coupled with sedimentation, results in a low therapeutic efficacy. Drugs can find it hard to fully diffuse in a urine-rich environment that is constantly swapping out fluids to remain clean. Additionally, it's difficult to get the medication in all corners of the bladder, which results in some cell layers being untreated.
이 소변은 침전과 결합되어 치료 효능이 낮아집니다. 깨끗한 상태를 유지하기 위해 지속적으로 체액을 교체하는 소변이 풍부한 환경에서는 약물이 완전히 확산되기 어려울 수 있습니다. 또한 방광의 모든 구석구석에 약물을 투여하는 것이 어렵기 때문에 일부 세포층이 치료되지 않는 결과를 낳습니다.
These untreated cells can become future tumors and lead to the patient having to undergo multiple procedures and monitoring to ensure effectiveness for the following 5 years after treatment. Thankfully, researchers have put many years into figuring out the best way to deliver these life-giving drugs, and this latest development shows massive potential.
이러한 치료되지 않은 세포는 미래의 종양이 될 수 있으며 환자는 치료 후 5년 동안 효과를 보장하기 위해 여러 절차와 모니터링을 거쳐야 합니다. 고맙게도 연구자들은 이러한 생명을 주는 약물을 전달하는 가장 좋은 방법을 찾기 위해 수년을 투자해 왔으며 이 최신 개발은 엄청난 잠재력을 보여줍니다.
Nanobots Study
나노봇 연구
The study, “Urease-powered nanobots for radionuclide bladder cancer therapy,” was published in Nature Nanotechnology. In the paper, scientists discuss the use of radiolabeled mesoporous silica-based urease-powered nanobots to improve bladder cancer treatment procedures. Specifically, the engineers wanted to see how the nanoparticles penetrated the bladder walls and dispersed across the organs.
"방사성 핵종 방광암 치료를 위한 우레아제 기반 나노봇"이라는 연구는 Nature Nanotechnology에 게재되었습니다. 논문에서 과학자들은 방광암 치료 절차를 개선하기 위해 방사성 표지된 메조다공성 실리카 기반 우레아제 기반 나노봇의 사용에 대해 논의합니다. 특히 엔지니어들은 나노입자가 어떻게 방광벽을 관통하여 장기 전체에 분산되는지 확인하고 싶었습니다.
Source – Bioengineering of Catalonia (IBEC) and CIC biomaGUNE.
출처 – IBEC(카탈로니아 생명공학) 및 CIC biomaGUNE.
Nanomachines
나노머신
The nanobots used in this experiment are shaped like porous spheres. They Are made of silica and are designed to self-propel when exposed to the protein urease, which is found in urine. The researchers monitored as the silica nanoparticles (MSNPs) moved about the organ, reaching the deepest corners. Specifically, the nanobots move using ammonia and CO2 created by the asymmetric decomposition of urease around the device.
이 실험에 사용된 나노봇은 다공성 구체 모양입니다. 이 제품은 실리카로 만들어졌으며 소변에서 발견되는 단백질 우레아제에 노출되면 자체 추진하도록 설계되었습니다. 연구진은 실리카 나노입자(MSNP)가 장기 주위를 이동하면서 가장 깊은 모서리에 도달하는 것을 모니터링했습니다. 구체적으로 나노봇은 장치 주변의 우레아제의 비대칭 분해로 생성된 암모니아와 CO2를 사용하여 움직입니다.
Test
시험
The testing phase involved two lab mice, vivo and ex vivo. Both mice suffered from bladder cancer tumors located deep within their organs. The researchers injected nanoparticles directly into the patients so the team could study the maneuverability of the nanoparticles and their accumulation within the organ. Notably, the mice were made to change position every 30 minutes to help facilitate equal dispersion across the organ. Here's what was learned.
테스트 단계에는 생체 내 및 생체 외 두 마리의 실험용 쥐가 포함되었습니다. 두 쥐 모두 장기 내부 깊숙한 곳에 방광암 종양이 있었습니다. 연구진은 나노입자를 환자에게 직접 주입하여 나노입자의 조작성과 장기 내 축적을 연구할 수 있었습니다. 특히, 장기 전체에 균등한 분산을 촉진하기 위해 쥐의 위치를 30분마다 바꾸도록 했습니다. 배운 내용은 다음과 같습니다.
Murine Tests
쥐 테스트
Murine tests were used to study the level of penetration achieved by the nanoparticles. To accomplish this task, the team used radio-iodinated nanobots. The team relied on the commonly used Iodine-131 and positron emission tomography (PET) imaging to see exactly what layers were treated.
나노입자에 의해 달성된 침투 수준을 연구하기 위해 쥐과 테스트가 사용되었습니다. 이 작업을 수행하기 위해 팀은 방사성 요오드화 나노봇을 사용했습니다. 팀은 일반적으로 사용되는 요오드-131과 양전자 방출 단층 촬영(PET) 영상을 사용하여 정확히 어떤 층이 처리되었는지 확인했습니다.
Optical System
광학계
The engineers created a new fluorescence microscopy system developed at IRB Barcelona. This new optical testing process provides an in-depth 3d model demonstrating penetration levels across the organ. Specifically, a system that used Label-free optical contrast based on polarization-dependent scattered light-sheet microscopy of cleared bladders made the process easier. It eliminated the light usually refracted by the liver, which made it much easier to confirm the nanoparticle's movement.
엔지니어들은 IRB Barcelona에서 개발된 새로운 형광 현미경 시스템을 만들었습니다. 이 새로운 광학 테스트 프로세스는 장기 전체의 침투 수준을 보여주는 심층적인 3D 모델을 제공합니다. 특히, 투명 방광의 편광 의존 산란광 시트 현미경 검사법을 기반으로 하는 무표지 광학 대비를 사용하는 시스템을 사용하면 프로세스가 더 쉬워졌습니다. 이는 일반적으로 간에서 굴절되는 빛을 제거하여 나노입자의 움직임을 훨씬 쉽게 확인할 수 있게 했습니다.
Results
결과
The test results were eye-opening. The new process was able to achieve far better dispersion and penetration versus traditional methods. Specifically, a single dose of urea-powered, radionuclide-carrying nanorobots successfully reduced the size of tumors in the test subjects by 90%. Interestingly, the team discovered that the nanobots were able to break down the wall of the bladder and the extracellular wall of the tumor by altering Ph levels.
테스트 결과는 놀라웠습니다. 새로운 공정은 기존 방법에 비해 훨씬 더 나은 분산과 침투를 달성할 수 있었습니다. 특히, 요소로 구동되는 방사성 핵종을 운반하는 나노로봇의 단일 용량은 테스트 대상의 종양 크기를 90%까지 성공적으로 줄였습니다. 흥미롭게도 연구팀은 나노봇이 Ph 수준을 변경하여 방광벽과 종양의 세포외벽을 파괴할 수 있다는 사실을 발견했습니다.
Benefits
이익
There are several benefits that the new bladder cancer study makes possible. For one, it shows enhanced diffusion and mixing capabilities. As such, it makes treatments more effective. The self-propelled nanobots can enter and spread across the bladder using urine as the catalyst, creating a more efficient approach.
새로운 방광암 연구가 가능하게 하는 몇 가지 이점이 있습니다. 우선, 향상된 확산 및 믹싱 기능을 보여줍니다. 따라서 치료가 더욱 효과적입니다. 자체 추진 나노봇은 소변을 촉매제로 사용하여 방광에 들어가 확산될 수 있어 보다 효율적인 접근 방식을 만들 수 있습니다.
Pierce Tumor Wall
피어스 종양 벽
The new process sent nanobots colliding with the urothelium. In the past
새로운 프로세스는 요로 상피와 충돌하는 나노봇을 보냈습니다. 과거에
부인 성명:info@kdj.com
제공된 정보는 거래 조언이 아닙니다. kdj.com은 이 기사에 제공된 정보를 기반으로 이루어진 투자에 대해 어떠한 책임도 지지 않습니다. 암호화폐는 변동성이 매우 높으므로 철저한 조사 후 신중하게 투자하는 것이 좋습니다!
본 웹사이트에 사용된 내용이 귀하의 저작권을 침해한다고 판단되는 경우, 즉시 당사(info@kdj.com)로 연락주시면 즉시 삭제하도록 하겠습니다.