|
|
 |
|
 |
|
 |
|
 |
|
 |
|
 |
|
 |
|
 |
|
 |
|
 |
|
 |
|
 |
|
 |
|
 |
|
新しい研究では、腫瘍を殺す薬をより効率的に患者に配布するためのナノボットの使用が検討されています。その結果は、今後の治療に多大な影響を与える可能性があります。
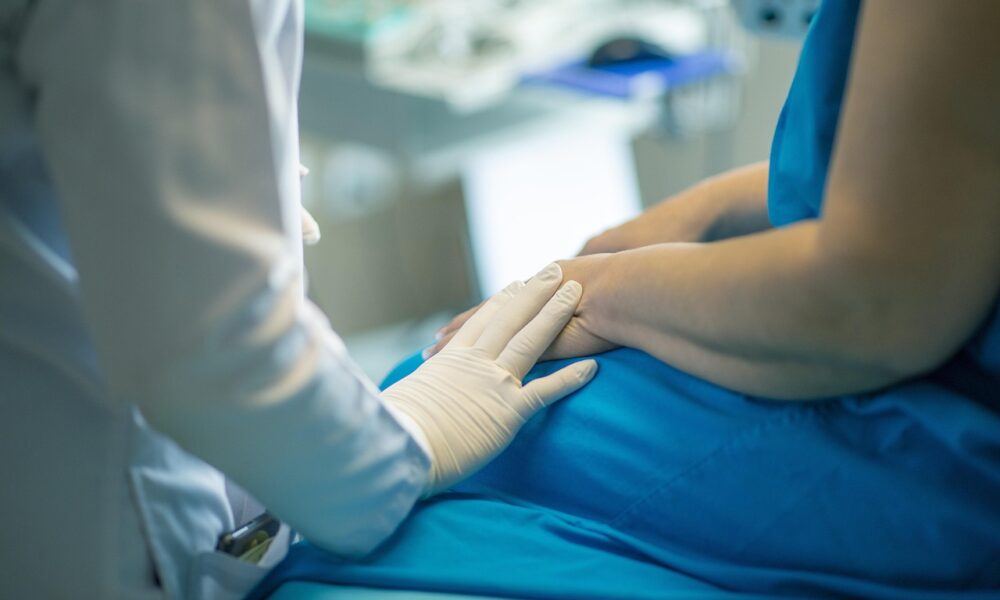
A new study explores the use of nanobots to distribute tumor-killing medications more efficiently to patients. The researchers employed tiny self-propelled machines that could penetrate deeper into bladder cancer tumors when compared to current methods. The results could have a resounding effect on treatment moving forward. Here's everything you need to know.
新しい研究では、腫瘍を殺す薬をより効率的に患者に配布するためのナノボットの使用が検討されています。研究者らは、現在の方法と比較して膀胱がん腫瘍の奥深くまで侵入できる小型の自走式機械を使用した。その結果は、今後の治療に多大な影響を与える可能性があります。知っておくべきことはすべてここにあります。
Bladder Cancer
膀胱がん
Bladder cancer is one of the leading causes of death around the world. A recent study by the American Cancer Society projected around 82K people will be diagnosed with bladder cancer in 2023 alone. Of those diagnosed, around 16.5K will not survive the ordeal. As such, it's easy to see why there's considerable effort put towards helping to reduce the number of people who will be affected by bladder cancer in the coming years.
膀胱がんは、世界中の主な死因の 1 つです。米国癌協会による最近の研究では、2023 年だけで約 82,000 人が膀胱癌と診断されると予測されています。診断された人のうち、約 16.5,000 人がこの試練を乗り越えることができません。したがって、今後数年間で膀胱がんに罹患する人の数を減らすために多大な努力が払われる理由は簡単にわかります。
The main causes of bladder cancer are smoking, workplace exposure to carcinogens, dietary factors, genes, diesel exhaust exposure, and radiotherapy. Notably, around 75% of confirmed bladder cancer tumors are non-muscle-invasive, meaning the cancer is located only on the inner layer of cells.
膀胱がんの主な原因は、喫煙、職場での発がん性物質への曝露、食事要因、遺伝子、ディーゼル排気への曝露、および放射線療法です。特に、確認された膀胱がん腫瘍の約 75% は非筋層浸潤性であり、これはがんが細胞の内層にのみ存在することを意味します。
Current Treatment
現在の治療法
The current methods of treating bladder cancer are effective and not dangerous. However, they leave lots of room for improvement. The most common procedure involves administering drugs directly to the bladder. The problem with treating bladders versus other organs is that it's designed to flush out toxins with urine constantly.
膀胱がんの現在の治療法は効果的であり、危険ではありません。ただし、改善の余地がたくさん残されています。最も一般的な処置には、膀胱に薬剤を直接投与することが含まれます。他の臓器と比較して膀胱を治療する場合の問題点は、膀胱が常に尿とともに毒素を排出するように設計されていることです。
This urine, coupled with sedimentation, results in a low therapeutic efficacy. Drugs can find it hard to fully diffuse in a urine-rich environment that is constantly swapping out fluids to remain clean. Additionally, it's difficult to get the medication in all corners of the bladder, which results in some cell layers being untreated.
この尿は沈降と相まって、治療効果が低くなります。清潔を保つために常に体液を交換している尿が豊富な環境では、薬物が完全に拡散するのは難しい場合があります。さらに、膀胱の隅々まで薬剤を届けることは困難であり、その結果、一部の細胞層が治療されないことになります。
These untreated cells can become future tumors and lead to the patient having to undergo multiple procedures and monitoring to ensure effectiveness for the following 5 years after treatment. Thankfully, researchers have put many years into figuring out the best way to deliver these life-giving drugs, and this latest development shows massive potential.
これらの未治療の細胞は将来腫瘍となる可能性があり、患者は治療後 5 年間の有効性を確保するために複数の処置とモニタリングを受けなければならないことになります。ありがたいことに、研究者たちは、これらの命を与える薬を投与する最良の方法を見つけることに何年も費やしており、この最新の開発は大きな可能性を示しています。
Nanobots Study
ナノボットの研究
The study, “Urease-powered nanobots for radionuclide bladder cancer therapy,” was published in Nature Nanotechnology. In the paper, scientists discuss the use of radiolabeled mesoporous silica-based urease-powered nanobots to improve bladder cancer treatment procedures. Specifically, the engineers wanted to see how the nanoparticles penetrated the bladder walls and dispersed across the organs.
この研究「放射性核種膀胱がん治療のためのウレアーゼを利用したナノボット」は、Nature Nanotechnology に掲載されました。論文の中で科学者らは、膀胱がんの治療手順を改善するための放射性標識メソポーラスシリカベースのウレアーゼを動力源とするナノボットの使用について議論している。具体的には、エンジニアらは、ナノ粒子がどのように膀胱壁を貫通し、臓器全体に分散するのかを確認したいと考えていました。
Source – Bioengineering of Catalonia (IBEC) and CIC biomaGUNE.
出典 – Bioengineering of Catalonia (IBEC) および CIC biomaGUNE。
Nanomachines
ナノマシン
The nanobots used in this experiment are shaped like porous spheres. They Are made of silica and are designed to self-propel when exposed to the protein urease, which is found in urine. The researchers monitored as the silica nanoparticles (MSNPs) moved about the organ, reaching the deepest corners. Specifically, the nanobots move using ammonia and CO2 created by the asymmetric decomposition of urease around the device.
この実験で使用されたナノボットは、多孔質の球のような形状をしています。これらはシリカでできており、尿中に含まれるタンパク質ウレアーゼにさらされると自走するように設計されています。研究者らは、シリカナノ粒子(MSNP)が臓器内を動き回り、最も深い隅に到達するのを観察した。具体的には、ナノボットは、デバイス周囲のウレアーゼの不斉分解によって生成されるアンモニアと CO2 を使用して移動します。
Test
テスト
The testing phase involved two lab mice, vivo and ex vivo. Both mice suffered from bladder cancer tumors located deep within their organs. The researchers injected nanoparticles directly into the patients so the team could study the maneuverability of the nanoparticles and their accumulation within the organ. Notably, the mice were made to change position every 30 minutes to help facilitate equal dispersion across the organ. Here's what was learned.
試験段階には、生体内および体外で 2 匹の実験用マウスが関与しました。両方のマウスは、臓器の深部に位置する膀胱癌腫瘍を患っていました。研究者らはナノ粒子を患者に直接注射し、ナノ粒子の操作性と臓器内でのナノ粒子の蓄積を研究した。注目すべき点は、臓器全体に均等に分散しやすくするために、マウスを 30 分ごとに位置を変えるようにしたことです。学んだことは次のとおりです。
Murine Tests
ネズミの検査
Murine tests were used to study the level of penetration achieved by the nanoparticles. To accomplish this task, the team used radio-iodinated nanobots. The team relied on the commonly used Iodine-131 and positron emission tomography (PET) imaging to see exactly what layers were treated.
ネズミの試験を使用して、ナノ粒子によって達成される浸透レベルを研究した。この課題を達成するために、チームは放射性ヨウ素化ナノボットを使用しました。研究チームは、どの層が処理されたかを正確に確認するために、一般的に使用されているヨウ素 131 および陽電子放出断層撮影 (PET) イメージングを利用しました。
Optical System
光学系
The engineers created a new fluorescence microscopy system developed at IRB Barcelona. This new optical testing process provides an in-depth 3d model demonstrating penetration levels across the organ. Specifically, a system that used Label-free optical contrast based on polarization-dependent scattered light-sheet microscopy of cleared bladders made the process easier. It eliminated the light usually refracted by the liver, which made it much easier to confirm the nanoparticle's movement.
エンジニアたちは、IRB Barcelona で開発された新しい蛍光顕微鏡システムを作成しました。この新しい光学検査プロセスは、臓器全体の浸透レベルを示す詳細な 3D モデルを提供します。具体的には、透明な膀胱の偏光依存散乱光シート顕微鏡法に基づくラベルフリー光学コントラストを使用するシステムにより、プロセスが容易になりました。通常肝臓で屈折する光が排除されたため、ナノ粒子の動きの確認がはるかに容易になりました。
Results
結果
The test results were eye-opening. The new process was able to achieve far better dispersion and penetration versus traditional methods. Specifically, a single dose of urea-powered, radionuclide-carrying nanorobots successfully reduced the size of tumors in the test subjects by 90%. Interestingly, the team discovered that the nanobots were able to break down the wall of the bladder and the extracellular wall of the tumor by altering Ph levels.
テスト結果は目を見張るものでした。新しいプロセスは、従来の方法と比較してはるかに優れた分散と浸透を達成することができました。具体的には、尿素を動力源とする放射性核種を運ぶナノロボットの単回投与により、被験者の腫瘍サイズを90%縮小させることに成功した。興味深いことに、研究チームは、ナノボットが Ph レベルを変えることによって膀胱壁と腫瘍の細胞外壁を破壊できることを発見しました。
Benefits
利点
There are several benefits that the new bladder cancer study makes possible. For one, it shows enhanced diffusion and mixing capabilities. As such, it makes treatments more effective. The self-propelled nanobots can enter and spread across the bladder using urine as the catalyst, creating a more efficient approach.
新しい膀胱がん研究によって可能になるいくつかの利点があります。 1 つは、拡散能力と混合能力が強化されていることです。そのため、治療がより効果的に行われます。自走式ナノボットは、尿を触媒として使用して膀胱に入り、膀胱全体に広がり、より効率的なアプローチを生み出すことができます。
Pierce Tumor Wall
腫瘍壁を貫通する
The new process sent nanobots colliding with the urothelium. In the past
新しいプロセスでは、ナノボットが尿路上皮に衝突しました。過去に
免責事項:info@kdj.com
提供される情報は取引に関するアドバイスではありません。 kdj.com は、この記事で提供される情報に基づいて行われた投資に対して一切の責任を負いません。暗号通貨は変動性が高いため、十分な調査を行った上で慎重に投資することを強くお勧めします。
このウェブサイトで使用されているコンテンツが著作権を侵害していると思われる場合は、直ちに当社 (info@kdj.com) までご連絡ください。速やかに削除させていただきます。